新型肌松剂拮抗药舒更葡糖的前世今生
发布日期:2020/10/20 9:13:08
现代麻醉药物的核心部分可以概括在三个方面:消除手术病人的意识、疼痛感觉和肌肉张力。简单地说手术病人在失去意识和疼痛感觉之后,为保证手术方便地实施,需要使用肌肉松驰药物协助气管插管并提供良好的手术视野。手术结束后,理想的恢复途径是机体能够将残留的肌松药和其他吸入或静脉麻醉药物短时间内分解和排泄出去,从而迅速地恢复病人的自主呼吸,肌肉功能和清醒状态,减少术后手术室的停留时间或重症监护室的护理时间。
多年来医药界为此进行了系统的研究,取得了非凡的成就,但是也应该看到,过去20年来,麻醉药物的研究进展与其他医药领域相比存在着一定的滞后现象。舒更葡糖(Sugammadex)的出现则开创了一个崭新的局面,给麻醉与手术医生和病人带来了前所未有的体验。

舒更葡糖是一种新型原创药,属于非去极化类固醇类肌松剂的拮抗药。静脉注射后,进入体内迅速结合血液中游离的罗库溴铵(Rocuronium),使后者组织细胞间的浓度迅速下降[1],重建了神经肌肉间的传递功能,从而迅速地恢复了病人的自主呼吸和肢体活动能力。
舒更葡糖的上市,标志着麻醉医生可以精准地控制肌肉松紧程度,为术后病人肌肉收缩功能的恢复提供了一条可控的路径。正如美国食品药物管理局(FDA)在其网站总结所述,舒更葡糖是2015年批准的药物之中货真价实的突破性新药(NoteworthyFirst-in-Class product)。它的上市,为麻醉界精准治疗开启了良好的开端。虽然舒更葡糖在美国的上市途径经历了曲折的道路,但是最终还是获得了FDA的首肯。在中国也已完成了临床试验,等待着国家药品监督管理局的批准。本文认为理解它的研发过程,作用机制可以更好地帮助麻醉医生在临床实践中的正确使用。
一、研发历程
先灵保雅2007年合并欧洲荷兰药物公司澳甘楼(Organon)之前,澳甘楼在苏格兰有一家称为纽豪斯的研药基地。纽豪斯有一很出名的神经肌肉研究小组,上世纪60年代以来,一直在研究速效短效类神经肌肉阻滞剂。临床上常用的非去极化类固醇类肌松药维库溴铵和罗库溴铵就是产于此地。
1994年罗库溴铵上市不久,因怀疑其对血管平滑肌有阻断作用,该小组邀请了邻近的Anton Bom(薄木)博士来协同研究这一课题。薄木是研究血管平滑肌的专家,知道罗库溴铵很难溶于水,需要在酸性条件下(pH4)溶解。薄木利用平滑肌研究中传统的有机溶剂来试图溶解罗库溴铵,竟然发现沒有一种溶剂可以成功地溶解罗库溴铵。于是他想起早年曾经用过环糊精(Cyclodextrins)来溶解类固醇类激素的先例。
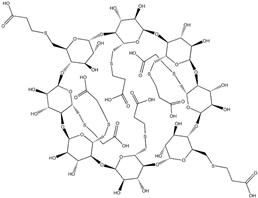
环糊精是一种环型多糖分子(图1),分子外部具有亲水性,环的中央有一个疏水的孔洞,亲脂的分子比如类固醇可以进入环孔中,形成一个水溶性复合物[2]。
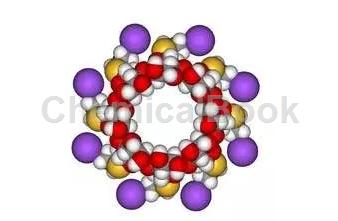
图1:舒更葡糖的分子构型
1997年的一天,薄木坐在办公室桌前,凝视着罗库溴铵的分子结构沉思(图2)。这是一个含有类固醇核心结构的药物,可不可以用环糊精结合罗库溴铵,从而消除血液和组织间游离的罗库溴铵?这样在麻醉苏醒期间,可以迅速地消除罗库溴铵拮抗乙酰胆碱受体的肌松作用,快速地恢复手术病人的自主呼吸[3]。这个想法一闪现,薄木禁不住莞尔一笑,一定要试一试这个好主意。功夫不负有心人,最初的实验表明环糊精的确可以套住罗库溴铵,但是套的不紧,罗库溴铵可以轻易地逃脱。
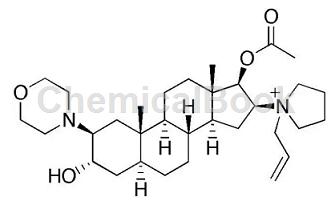
图2:罗库溴铵的分子结构
有了这样的初步结果,薄木的信心大增,看来需要做点工作来增加罗库溴铵与舒更葡糖的亲和力。环糊精的中央孔洞可能小了一点,应该在每个糖分子上加些侧链来扩大孔径。这个想法的关键点是要确保所加的侧链不能进入孔内引起干扰,如果侧链带上负电荷则可以做到这一点。改良的环糊精侧链上的负电荷可以与罗库溴铵氮原子上的正电荷紧密结合而形成牢固的复合物。这个令人兴奋的设想吸引了另一位医药化学家张明強博士,他首先搜寻了市场上可以买到的环糊精分子,通过体内和体外一系例药理实验,设法找到了化学结构的样板,经过筛选,最终合成了一系列新型环糊精衍生物[4]。
药物研究经常出现歪打正着的现象,就是最终的研发产品往往有些偏离最初的预想。当初研发舒更葡糖的目的是为了选择性与罗库溴铵结合,后来发现另外两个类固醇类肌松药也可以结合舒更葡糖,比如泮库溴铵和维库溴铵,只是亲和力相对较低。但是其他类型的肌松药则无亲和力,比如琥珀胆碱或阿曲库胺苯磺酸盐类。进一步的研究发现一个舒更葡糖分子可以通过非共价键方式结合一个类固醇类肌松药分子,因而具有一对一的拮抗关系[5,6]。
1999年3月,批筛选的药物出笼,其中含有Org25969,就是今天上市的舒更葡糖。舒更葡糖的药理特性非常突出,很快成为筛选药中的领头羊。为此2001年,使用环糊精这一方法和舒更葡糖这一类洐生药物以及合成方法都进行了专利申请。同年开展了临床试验,验证药物的临床效应,2005年发表了这一试验结果[6],使用正常插管剂量的罗库溴铵(0.6 my/kg)后,给予舒更葡糖8 mg/kg进行拮抗,只需3分钟就可以完全逆转前者的肌松效应。
二.FDA的挑战
舒更葡糖的上市批准之路,在欧洲与美国截然不同。2007年申报之后,欧盟于2008年迅速地批了下来,而美国的FDA批准之路则是一波多折,三进三出,直到第四次重新申请,方于2015年底首获FDA批准,此时距离次预批时间已经间隔了8个年头。
FDA为什么设下如此多的关卡呢?是药效问题还是副作用问题?
早在2008年8月次批准前,FDA专家委员会进行了首次审查,以全票通过向FDA推荐批准,可是FDA并未采纳专家的建议,发出了不予批准的通知。FDA主要的忧虑有以下几点:
1)在最初申报的材料中,有1例过敏反应和31例超敏反应,如果重复使用该药,那么药物的超敏和过敏反应发生的几率是多少?潜在的副作用机制是什么呢?
2)在体内体外药理实验中,发现活化部分凝血活酶时间(activated Partial Thromboplastin Time,aPTT)和血浆凝血酶原时间(Prothrombin Time, PT)有一定的延长[7],需要进一步实验评估舒更葡糖对外科手术出血的影响;
3)需要澄清舒更葡糖对心律失常和QT时间的效应。
为了完好地回答FDA的提问,先灵保雅设计了4个试验来评估舒更葡糖对出凝血的作用,新的试验表明舒更葡糖在使用开始时,几分钟内轻度延长aPTT/PT,但是这种效应在1小时内逐渐消失。此外,在大规模髋关节和膝关节置换术的病人中,并没有观察到出血异常或输血增多的现象[7]。针对心律失常的问题,通过进一步分析临床2期和3期的试验数据以及欧盟等国批准后的临床使用数据[8,9],结果表明使用舒更葡糖之后并没有延长QT时间,且与新斯的明相比,心律失常并未增多。最后在健康人中做了一个随机双盲对照试验,借以测定舒更葡糖使用后的过敏反应发生率[10]。
这些临床试验又花了三年多的时间才得以完成,此时先灵保雅已经与默沙东合并,合并后的默沙东于2012年又重新申请了新药批准。2013年9月,FDA做出了否定的裁决。FDA指出在超敏反应的临床试验中有违反操作程序的行为,因而获得的试验结果是不可靠的。但是认为出血和心律失常的疑问已经得到圆满的解答。2014年,第三次新药申请又送到了FDA。
此次临床试验是在375位清醒志愿者中进行的,受试者分别接受4 mg/kg,16 mg/kg舒更葡糖或生理盐水,观察他们的过敏反应和超敏反应。在16 mg/kg组中出现1例过敏反应,但无低血压、哮鸣或针对舒更葡糖的IgG/IgE抗体,说明发生的机制不明了。但在临床试验中,3519例病人使用舒更葡糖后无一例产生过敏反应。最后从欧洲批准后的临床使用总结中发现,截止2015年3月31日,1150万使用者中有273例过敏反应,237例需要进行常规处理[10]。
2015年4月,FDA又一次发出否定的裁决。FDA发现在超敏反应的一个试验中心,工作人员违反了双盲试验的原则。FDA要求重新审查其他试验中心并对数据进行重新分析。11月又重新召集专家审议,审查了新的数据和大规模临床使用后的数据,专家们又一次全票通过推荐批准[11]。至此,经过8年的风风雨雨,舒更葡糖终于在2015年12月16日获得FDA的批准,此时澳甘楼,先灵保雅两公司已于7年前消失在合并的潮流中了,舒更葡糖目前属于默沙东公司的原创新药。
参考文献:
[1]EpemoluO, Bom A, Hope F, Mason R. Reversal of Neuromuscular Blockade and SimultaneousIncrease in Plasma Rocuronium Concentration after the Intravenous Infusion ofthe Novel Reversal Agent Org25969. Anesthesiology 2003; 99:632–637
[2]GijsenberghF, Ramael S, Houwing N, van Iersel T. First human exposure of Org 25969, anovel agent to reverse the action of rocuronium bromide. Anesthesiology 2005; 103:695–703
[3]de BoerHD, van Egmond J, de Pol F, Bom A, Booji LHDJ. Reversal of profound rocuroniumneuromuscular blockade by sugammadex in rhesus monkeys. Anesthesiology 2006;104:718–723
[4]DanielDirkmann, Dr. med., Martin W. Britten, Henning Pauling, Dr. med., JulianeWeidle, Dr. med., Lothar Volbracht, Dr. med., Klaus Görlinger, Dr. med., JürgenPeters, Prof. Dr. med.. Anticoagulant Effect of Sugammadex: Just an In VitroArtifact. Anesthesiology 2016; 124(6):1277-1285
[5]SchallerSF, Fink H. Sugammadex as a reversal agent for neuromuscular block: anevidence-based review. Core Evid 2013; 8:57–67
[6]KopmanAF. Sugammadex: A Revolutionary Approach to Neuromuscular Antagonism.Anesthesiology 2006; 104:631-633
[7]Rahe-MeyerN, Fennema H, Schulman S, Klimscha W, Przemeck M, Blobner M, Wulf H, Speek M,McCrary Sisk C, Williams-Herman D, Woo T, Szegedi A. Effect of reversal ofneuromuscular blockade with sugammadex versus usual care on bleeding risk in arandomized study of surgical patients. Anesthesiology 2014; 121:969–977
[8]de KamPJ, Kuijk JV, Smeets J, Thomsen T, Peeters P. Sugammadex is not associated withQT/QTc prolongation: methodology aspects of an intravenousmoxifloxacin-controlled thorough QT study. Int J Clin Pharmacol Ther 2012; 50:595–604
[9]de KamPJ, Grobara P, Dennie J, Cammu G, Ramael S, Jagt-Smook ML, van den Heuvel MW,Berg RJ, Peeters PA. Effect of sugammadex on QT/QTc interval prolongation whencombined with QTc-prolonging sevoflurane or propofol anaesthesia. Clin DrugInvestig 2013; 33:545–551
[10]MerckSharp, Dohme Corp. A study to evaluate the incidence of hypersensitivity afteradministration of sugammadex in the healthy participants (MK-8616-101). InClinicalTrials.com: http://clinicaltrials.gov/show/NCT02028065. NLM identifier:NCT02028065
[11]MerckSharp, Dohme Corp. NDA 22225: Sugammadex Injection Anesthetic and AnalgesicDrug Products Advisory Committee (AC) Meeting: Sugammadex Advisory CommitteeBriefing Document, Kenilworth, NJ, November 6, 2015
欢迎您浏览更多关于舒更葡糖的相关新闻资讯信息